Египет утвердил использование китайской вакцины от Sinopharm
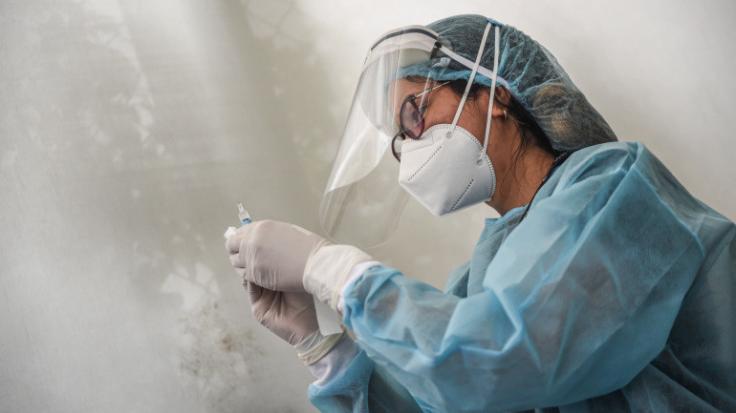
По словам министра здравоохранения, Египет предоставил нормативное разрешение на использование вакцины COVID-19, разработанной китайским фармацевтическим гигантом Sinopharm, и ожидается, что кампания по вакцинации начнется в конце января.
«В субботу египетские фармацевтические власти одобрили китайскую вакцину Sinopharm», - сказала Хала Зайед местному каналу MBC Masr.
Зайед отметила, что первая партия вакцины была доставлена в декабре, а новые дозы ожидаются в этом месяце.
«Вторая партия вакцины должна прибыть во вторую или третью неделю января, и как только она прибудет, мы начнем вакцинацию», - сказал министр.
Каждая партия вакцины состоит из 50 000 доз. Египет планирует закупить 40 миллионов доз препарата Sinopharm.
Министерство здравоохранения объявило, что первой группой, которой сделают вакцинацию, будут медицинские работники страны.
Источник: Al Jazeera